遥遥领先:CAR-T治疗实体瘤客观缓解率较美国标准治疗提高30倍!
导览
2024年5月7日-11日,第27届美国基因与细胞治疗学会(ASGCT)年会在美国马里兰州巴尔的摩召开。ASGCT成立于1996年,是全球基因和细胞治疗领域最大的专业性非营利医学和科学组织,在全球拥有超过5000名成员。ASGCT年会是全球基因与细胞治疗领域规模最大最具权威性的学术会议。
斯丹赛生物技术有限公司(以下简称斯丹赛),是一家专注于开发实体瘤CAR-T细胞治疗产品的临床阶段生物技术公司,公司关于实体肿瘤领先疗法GCC19CART的研究摘要荣幸入选了本次ASGCT年会。当地时间5月8日下午,斯丹赛首席技术官Victor Lu博士代表公司出席,并以口头报告的形式展示了GCC19CART美国临床试验CARAPIA-1的最新进展。GCC19CART是斯丹赛基于自主研发的CoupledCAR平台技术开发的首发候选产品,用于治疗复发/难治性转移性结直肠癌(R/R mCRC)患者。
斯丹赛参会信息
·摘要标题:A phase 1 dose escalation study of a novel coupled CAR T cell therapy, GCC19CART, for patients with metastatic colorectal cancer(GCC19CART的I期剂量递增研究,一种用于转移性结直肠癌患者的新型coupled CAR T细胞疗法)
·会议环节:Genetically Modified Immune Cells for AML and Solid Tumors
·会场:339-342
·摘要展示号:141

关于GCC19CART
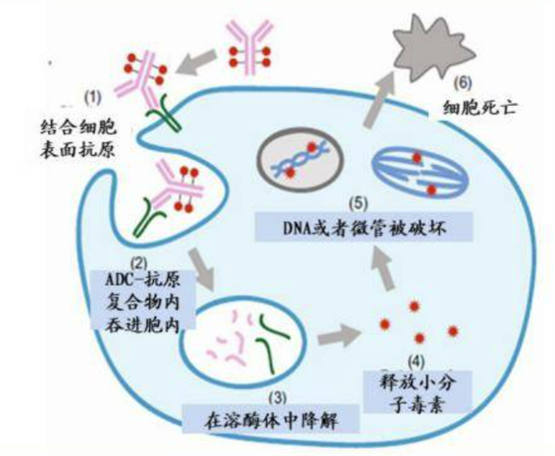
GCC19CART是以GCC为靶点,专门设计用于靶向治疗晚期结直肠癌的一款自体CAR-T产品。一项在中国进行的由研究者发起的多中心I期剂量爬坡临床试验显示,根据实体肿瘤疗效评价标准(RECIST1.1),GCC19CART低剂量组(1x10^6 CAR-T/kg)的客观缓解率(ORR)为15.4%(2/13),中剂量组(2x10^6 CAR-T/kg)的ORR为50%(4/8)。
2022年8月GCC19CART在美国启动Ⅰ期临床试验,该临床试验与美国几家著名医疗中心合作进行,包括Dana Farber(哈佛大学丹娜·法伯癌症研究所)、UCSF(加利福尼亚大学旧金山分校)肿瘤中心、University of Colorado(科罗拉多大学)肿瘤中心和COH(希望之城癌症中心)。截至2023年11月1日,低剂量组(1x10^6 CAR-T/kg)共有4名患者入组,患者已接受回输治疗并完成评估。经过美国第三方独立评估,按照RECIST1.1标准,低剂量组2名患者达到部分缓解(PR),ORR为50%(该结果优于同一剂量组的中国临床研究数据),临床疗效大大优于美国FDA 批准的三线标准疗法(ORR仅为1%-1.6%)。低剂量组临床试验已完成,中剂量组(2x10^6 CAR T/kg)临床试验正在进行中。截至2024年4月18日,中剂量组已有3名患者完成回输治疗,2名患者完成评估,其中1名患者达到PR。
美国I期临床试验的初步结果表明,GCC19CART在复发/难治性转移性结直肠癌中具有显著的临床疗效和良好的安全性;结合中国的临床研究数据可以看出,临床疗效与剂量呈正相关。该试验仍在进行中,临床试验编号:NCT05319314。
关于斯丹赛
斯丹赛生物技术有限公司是一家专注于开发实体瘤CAR-T细胞治疗产品的临床阶段生物技术公司。斯丹赛独特的CoupledCAR平台技术旨在克服治疗实体瘤的关键挑战,基于该平台技术开发的CAR-T产品已经在治疗晚期实体瘤(如结直肠癌)中取得了可喜的临床结果。公司针对晚期结直肠癌的CAR-T细胞治疗产品GCC19CART于2021年8月获得了美国食品和药物管理局(FDA)的临床试验批件,并于2022年4月获得FDA授予的快速通道资格,目前美国临床试验CARAPIA-1正在进行中,临床试验编号:NCT05319314。斯丹赛同时也在布局针对其它实体瘤(包括前列腺癌、胰腺癌等)的丰富的CAR-T候选药物管线。欲了解更多信息,请访问www.ictbio.com。
投资者联系方式
邮箱:ir@ictbioinc.com
联系电话:021-58959719